呼吸机出口指南
一、产品介绍和分类
呼吸机是现代临床医学中预防和治疗呼吸衰竭,减少并发症,挽救及延长病人生命的至关重要的医疗设备。呼吸机为无法呼吸或呼吸困难的患者提供协助,比鼻腔插管或氧气面罩提供更多的氧气。新冠患者进入ICU的最常见原因是严重的低氧性呼吸衰竭,该情况一般需要机械辅助呼吸,使用呼吸机在很大程度上有效提高新冠肺炎患者的存活率。
目前,我国未出台统一广泛使用的呼吸机分类标准。通常按照用途,呼吸机可分为成人、婴儿和新生儿、辅助呼吸和治疗用、麻醉、携带式急救和高频正压等六类。按照连接方式,可分为有创和无创两类。按照应用环境,可分为医用和家庭用两类。
近期出口欧盟、美国的多为用于成人、辅助呼吸和治疗、麻醉等用途的医用呼吸机。
二、出口通关要求
1. 商品归类

关联提示:
自3月11日起,美国取消部分医疗物资进口关税,其中包括呼吸机。企业可通过网址https://hts.usitc.gov/验证相关产品税率。
2. 禁限管理
商务部 海关总署 国家药品监督管理局2020年第5号《关于有序开展医疗物资出口的公告》:自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。
目前公告的具有呼吸机出口资质的企业名单如下:
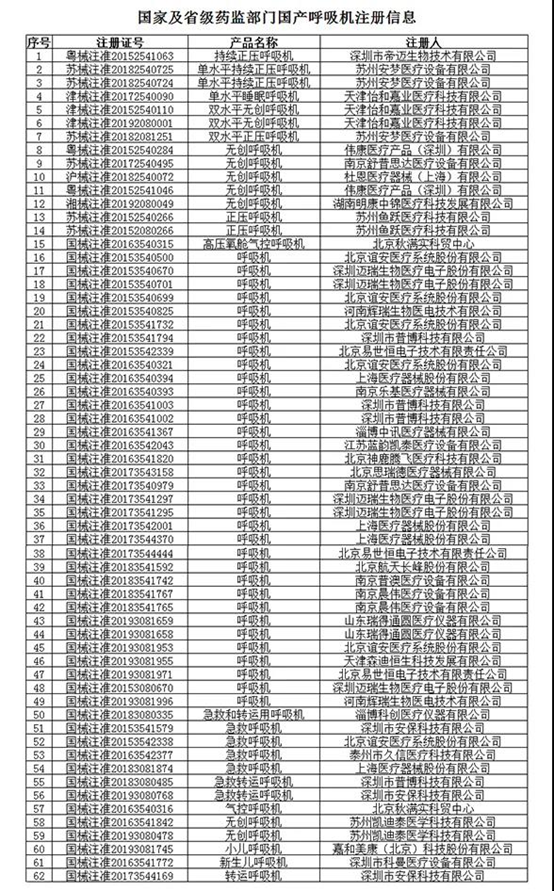
*该名单在国家药监局网站www.nmpa.gov.cn动态更新。
3. 出口退税
呼吸机及其零件、附件的出口退税率为13%。
三、各国准入条件
1. 美国
出口美国需FDA注册。国外的医疗器械必须指定一位美国代理人,该代理人负责紧急情况和日常事务交流。
2. 欧盟
出口欧盟需获得FSC(自由销售证书),该证书由唯一被欧盟指令授权的资质机构——欧洲经济区(EEA)的医疗器械主管机关出具。如企业产品已经获得CE标志,并已进行相关注册,出口欧盟不需要FSC,但出口欧洲经济区内其他非欧盟国家的,需提供FSC。
3. 日本
出口日本需PMDA注册。国外制造商必须向PMDA注册制造商信息。日本医药品和医疗器械综合机构(PMDA)网址:www.pmda.go.jp
4. 韩国
出口韩国需韩国卫生福利部下属食品药品安全部KFDA注册。韩国药监局Korea Pharmaceutical Traders Association网址:www.kpta.or.kr
韩国卫生福利部负责食品、药品、化妆品和医疗器械管理,下属食品药品安全部负责医疗器械管理。
5. 澳大利亚
出口澳大利亚需卫生部下属治疗商品管理局TGA注册。TGA网址:https://www.tga.gov.au/
澳大利亚产品分类与欧盟基本一致,如企业产品已经获得CE标志,可以简化TGA注册程序。
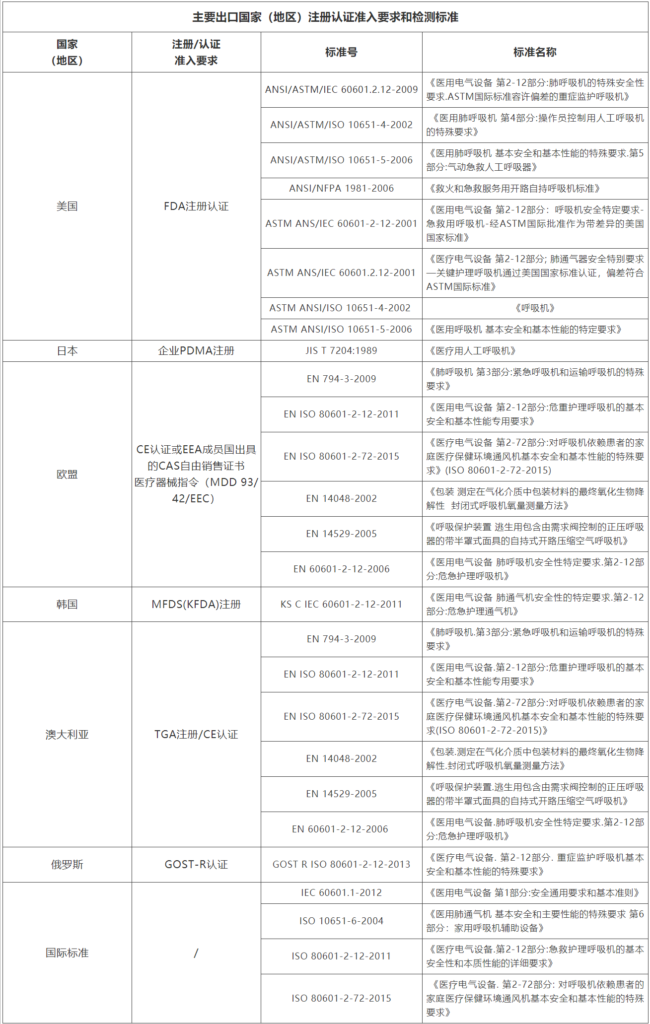
* 以上技术标准为各国进口或销售时,由各国海关或相关部门要求验核;如有动态调整,以相关标准管理机构官方发布为准,仅仅作为提醒或参考资料
四、国内外标准
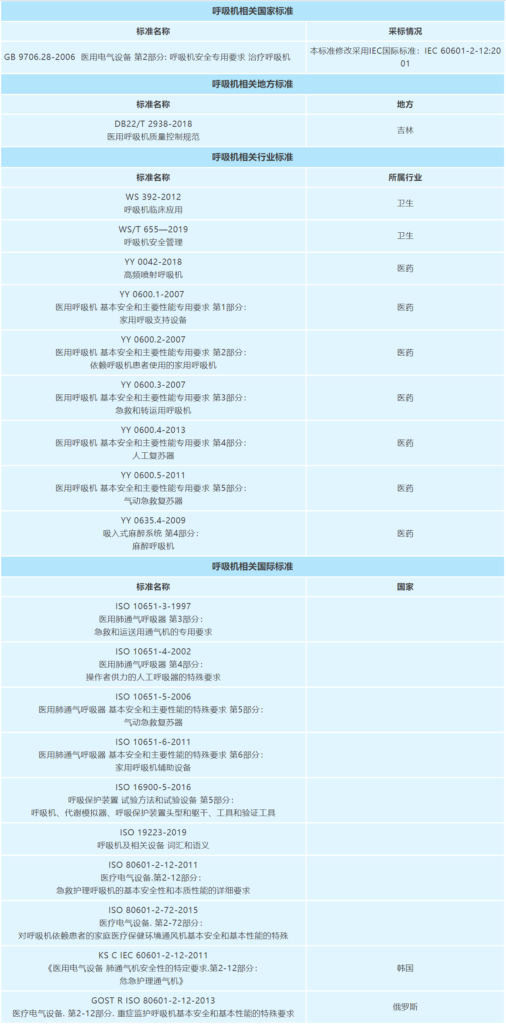
根据比对结果,目前包括中国在内的主要国家所制定的呼吸机标准技术内容及标准较一致,标准的国际通用程度较高,技术指标上差异性较小。

